Il test Prosigna, progettato sulla base della biologia del cancro al seno, fornisce la sicurezza per aiutare a fare le scelte giuste.
Conoscere e avere fiducia nella misurazione del rischio di recidiva è una considerazione importante per decidere quale trattamento raccomandare nel tumore della mammella HR+/HER2-.1

Il Prosigna Breast Cancer Assay è destinato alle donne in post-menopausa con tumore della mammella HR+ e HER2- in stadio iniziale.
Il Prosigna Prognostic Gene Signature Assay è un test di 2a generazione che ha mostrato performance superiori rispetto ai test genomici precedenti.
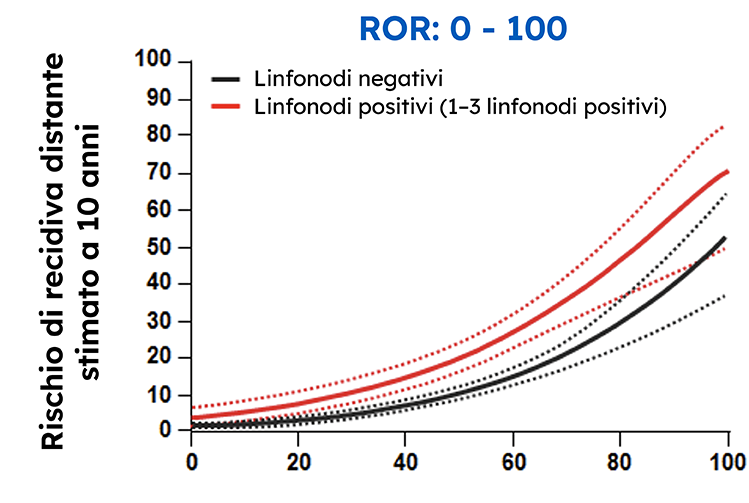
Il punteggio del rischio di recidiva (ROR) Prosigna aggiunge informazioni prognostiche significative ai fattori di rischio convenzionali come l’analisi anatomopatologica del tumore della paziente e i marcatori proteici rilevati mediante l’immunoistochimica.2
fornisce informazioni prognostiche più accurate sul rischio di recidiva distante tra l’espressione genica e i biomarcatori immunoistochimici.2
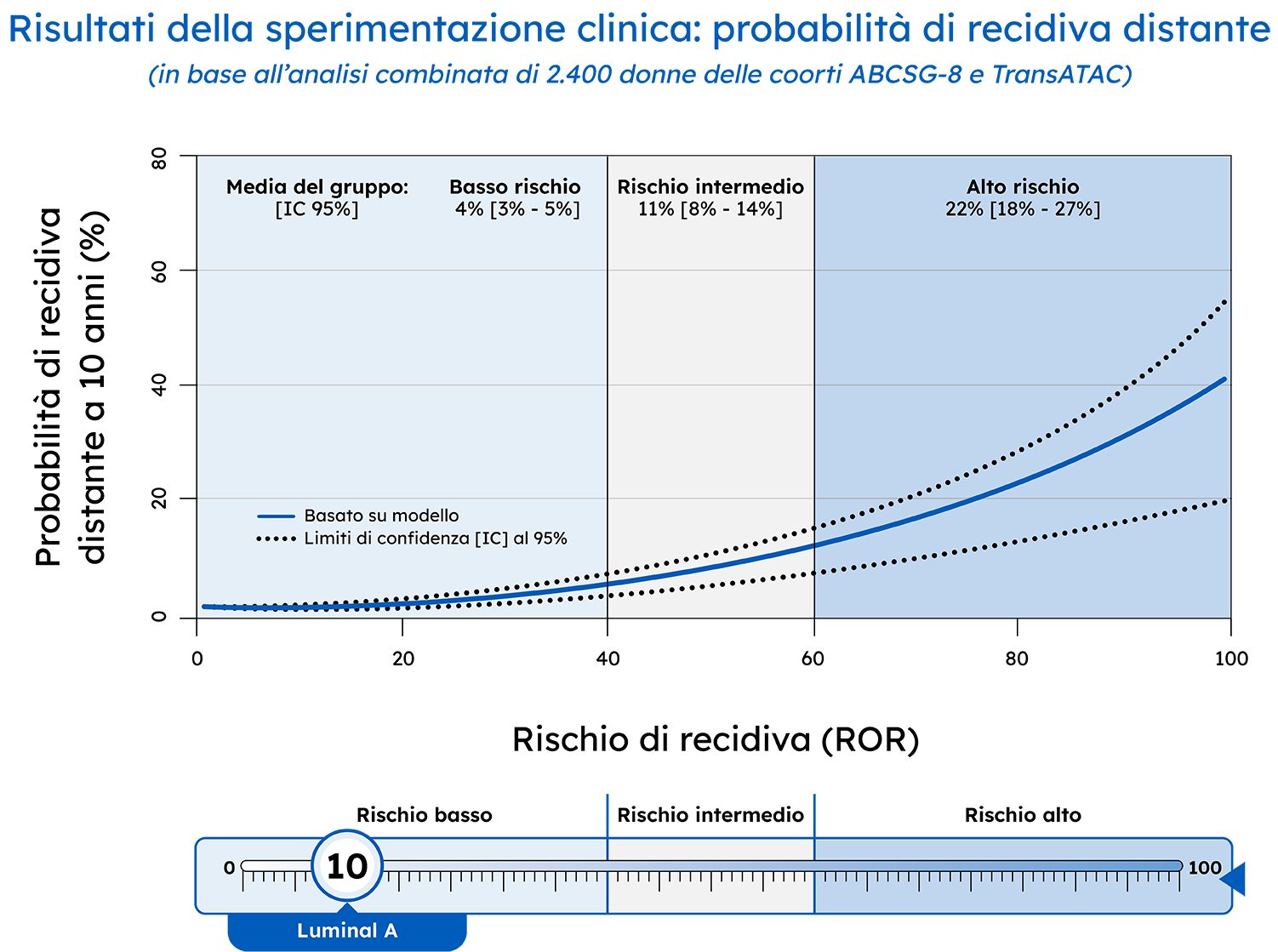
Il test Prosigna classifica accuratamente le pazienti con rischio di recidiva distante basso, intermedio o alto
Visualizza il rapporto annotato del paziente Prosigna
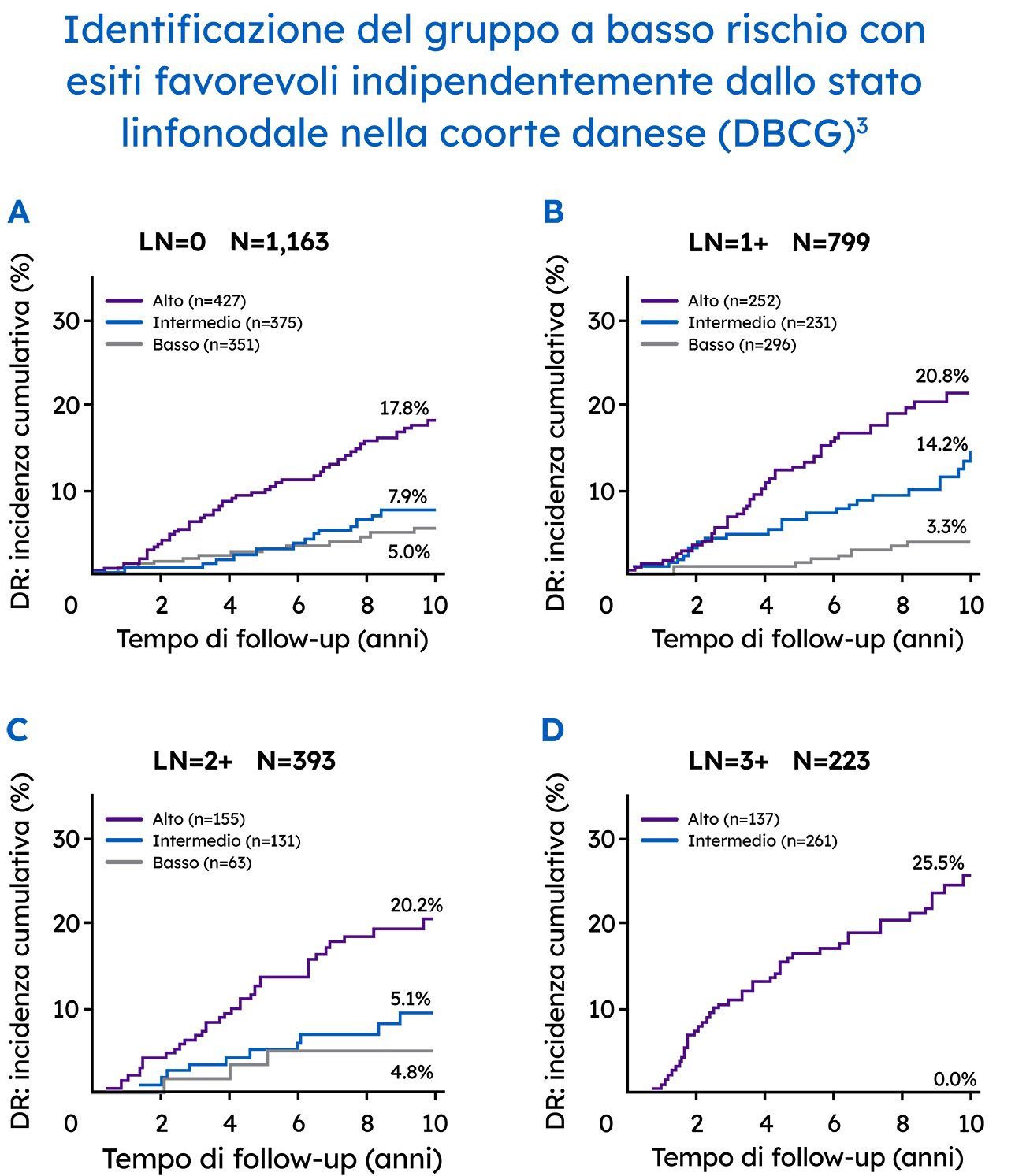
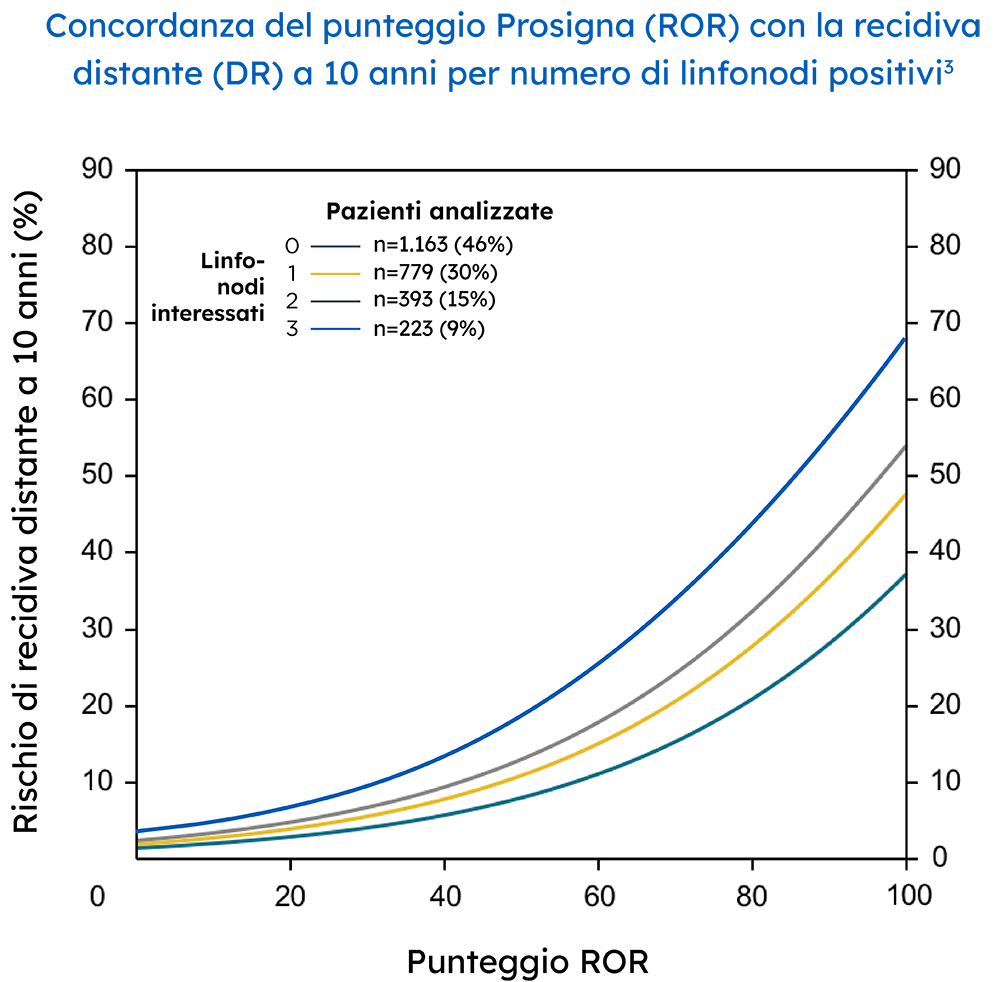 In un contesto reale, il test Prosigna ha identificato in modo affidabile pazienti a basso rischio con linfonodi negativi o che avevano da uno a tre linfonodi positivi, il che ha potuto aiutare i medici a decidere se una paziente poteva evitare in sicurezza la chemioterapia adiuvante.3 Il Danish Breast Cancer Cooperative Group (DBCG) ha esaminato le recidive a distanza in una coorte nazionale completa composta da 2.558 donne in postmenopausa con tumore della mammella in fase iniziale positivo ai recettori ormonali trattate con 5 anni di sola terapia endocrina.3
In un contesto reale, il test Prosigna ha identificato in modo affidabile pazienti a basso rischio con linfonodi negativi o che avevano da uno a tre linfonodi positivi, il che ha potuto aiutare i medici a decidere se una paziente poteva evitare in sicurezza la chemioterapia adiuvante.3 Il Danish Breast Cancer Cooperative Group (DBCG) ha esaminato le recidive a distanza in una coorte nazionale completa composta da 2.558 donne in postmenopausa con tumore della mammella in fase iniziale positivo ai recettori ormonali trattate con 5 anni di sola terapia endocrina.3
Il punteggio ROR Prosigna ha stimato in modo più accurato la probabilità di recidiva distante a 10 anni in questa popolazione rispetto alla stratificazione del rischio fornita da altri pannelli genici.3.4
Una prognosi accurata è fondamentale per le raccomandazioni di un trattamento a lungo termine
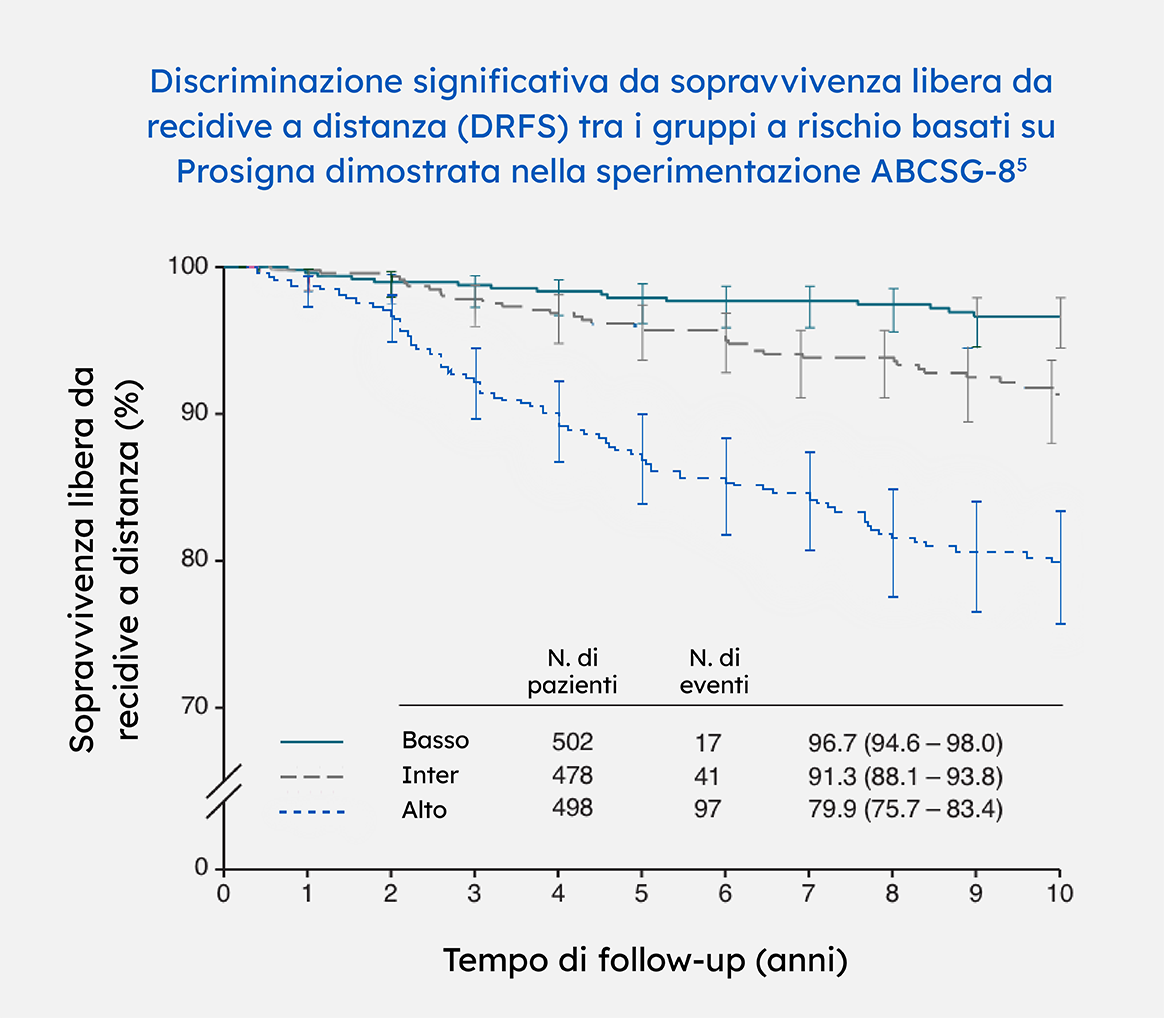 Ampia evidenza globale di validità clinica e utilità clinica in oltre 5.200 pazienti trattate con 5 anni di terapia ormonale standard e follow-up a 10 anni (prospettico e di popolazione)
Ampia evidenza globale di validità clinica e utilità clinica in oltre 5.200 pazienti trattate con 5 anni di terapia ormonale standard e follow-up a 10 anni (prospettico e di popolazione)
La differenziazione a basso e ad alto rischio è un fattore chiave per determinare una decisione terapeutica sicura
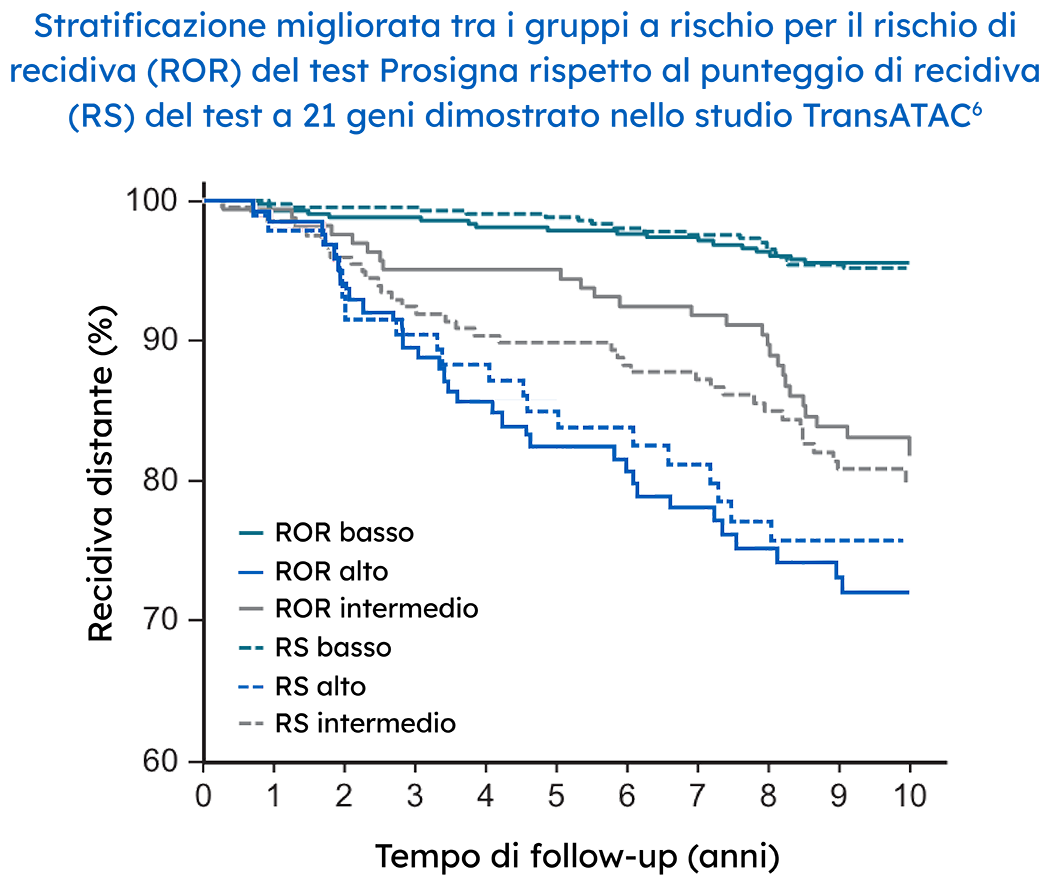 I risultati del rischio di recidiva di più della metà (59%) delle pazienti nella sottoanalisi di 663 dei 774 campioni originali all’interno dello studio TransATAC erano discordanti tra il test Prosigna e l’Oncotype Dx. I risultati osservati erano più coerenti con la categoria di rischio Prosigna, non con la categoria di rischio Oncotype Dx.6
I risultati del rischio di recidiva di più della metà (59%) delle pazienti nella sottoanalisi di 663 dei 774 campioni originali all’interno dello studio TransATAC erano discordanti tra il test Prosigna e l’Oncotype Dx. I risultati osservati erano più coerenti con la categoria di rischio Prosigna, non con la categoria di rischio Oncotype Dx.6
Il test Prosigna fornisce informazioni prognostiche accurate
Identificare le pazienti che possono evitare in sicurezza un trattamento eccessivo
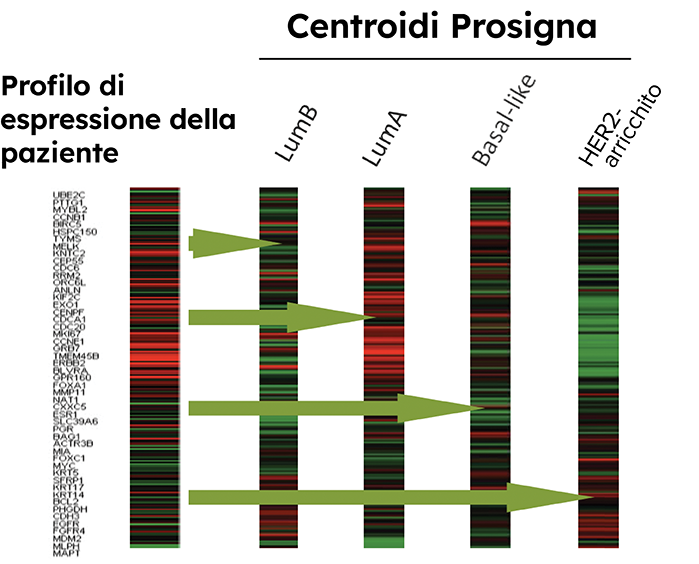
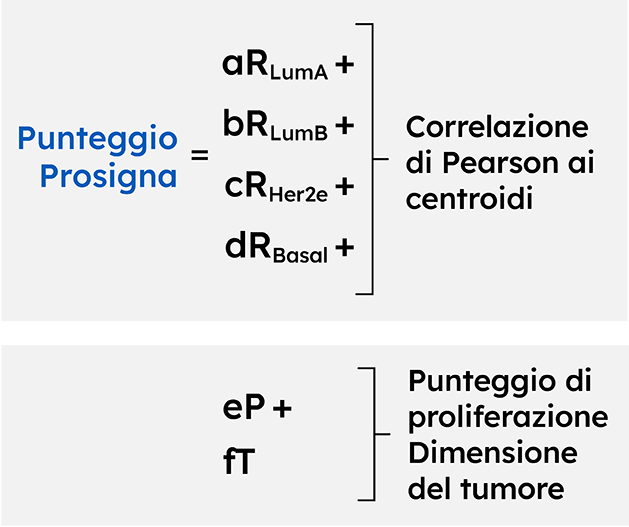
Il Prosigna Gene Expression Assay è l’unico test prognostico del tumore della mammella sviluppato dai quattro sottotipi molecolari PAM50.9
La classificazione nei sottotipi intrinseci consente una valutazione più accurata dei modelli di espressione genica del tumore.10

Vi è una notevole discordanza tra il sottotipo basato su IHC e i sottotipi molecolari di Prosigna.10
Gli esiti delle pazienti basati sui sottotipi molecolari sono stati valutati in un confronto testa a testa con l’IHC e il test Prosigna si è dimostrato più accurato.6 Errori nell’assegnazione del sottotipo possono influenzare in modo significativo il trattamento e gli esiti del tumore della mammella (Consenso degli esperti internazionali di St. Gallen11).
Prosigna è raccomandato insieme ad altre variabili clinico-patologiche per guidare le decisioni sulla terapia sistemica adiuvante per le donne con ESBC linfonodo negativo.
Prosigna è riconosciuto con evidenza di livello I, in parità con altri test di espressione genica consolidati. Si raccomanda l’uso di sottotipi molecolari basati su PAM50 per predire il beneficio della chemioterapia neoadiuvante.
Prosigna ha ricevuto il punteggio più elevato tra tutti i test prognostici negli anni 1–5 per ER+, HER2-, pN0 e pN+ EBC.
Prosigna ha avuto il massimo livello di punteggio tra tutti i test per la recidiva tardiva (anni 5–10)
I sottotipi PAM50 sono riconosciuti come predittivi da questo organismo.
Prosigna è raccomandato come opzione per guidare le decisioni sulla chemioterapia adiuvante per le persone con tumore della mammella HR+/HER2- con linfonodi negativi (LN).
Prosigna® Breast Cancer Prognostic Gene Signature Assay (test Prosigna) per l’uso sul sistema di analisi nCounter® è marcato CE per uso diagnostico in vitro nella prognosi e nella resezione chirurgica. Fare riferimento ai fogli illustrativi specifici della regione per le rispettive dichiarazioni sui prodotti.
Prosigna® in combinazione con il sistema di analisi nCounter® è marcato CE per l’uso diagnostico in vitro nelle donne in post-menopausa con tumore della mammella positivo al recettore ormonale (HR+), con linfonodi negativi, stadio I o II e nelle donne in post-menopausa con tumore della mammella positivo al recettore ormonale (HR+), con linfonodi positivi (1–3 linfonodi positivi), stadio II e IIIA da trattare con terapia endocrina adiuvante. Vedere il foglietto illustrativo per ulteriori dettagli su prosigna.com. ©2021 Veracyte, Inc. Prosigna e il logo Prosigna sono marchi commerciali e/o marchi registrati di Veracyte, Inc. in varie giurisdizioni.
ASCO ed ESMO sono marchi di fabbrica dell’American Society of Clinical Oncology e della European Society for Medical Oncology. National Institute for Health and Care Excellence (NICE), St Gallen International Consensus Panel, ASCO ed ESMO non approvano alcun prodotto o terapia.

Chirurgia: chirurgia conservativa della mammella (BCS) e biopsia del linfonodo sentinella (SLNB)
Patologia: carcinoma duttale infiltrante (IDC) grado III 15 mm
Tumore relativamente piccolo
Sottotipo: Luminal A
Punteggio del rischio di recidiva (ROR) Prosigna: 25
Gruppo di rischio Prosigna: 4%, basso rischio

Chirurgia: chirurgia conservativa della mammella (BCS) e biopsia del linfonodo sentinella (SLNB)
Patologia: carcinoma duttale infiltrante (IDC) grado III 17 mm
Tumore relativamente piccolo con biologia sfavorevole
Sottotipo: Luminal B
Punteggio del rischio di recidiva (ROR) Prosigna: 70
Gruppo di rischio Prosigna: 21%, alto rischio

Chirurgia: chirurgia conservativa della mammella (BCS) e biopsia del linfonodo sentinella (SLNB)
Patologia: carcinoma duttale infiltrante (IDC) grado III 15 mm
Tumore di medie dimensioni
Sottotipo: Luminal A
Punteggio del rischio di recidiva (ROR) Prosigna: 8
Gruppo di rischio Prosigna: 5%, basso rischio


Per ordinare il Prosigna Prognostic Gene Signature Assay, contattare Veracyte all’indirizzo [email protected]
References: 1. Alexandre M, et al. Cancer Manag Res. 2019;11:10353–10373. 2. Sestak I, et al. JAMA Oncol. 2018;4(4):545–553. 3. Lænkholm AVet al. J Clin Oncol. 018;10;36(8):735-740. 4. Costa et al. J Clin Oncol. 2018;10;36(8):725-727. 5. Gnant M, et al. Ann Oncol. 2014;25(2):339-45.6. Dowsett M, et al. J Clin Oncol. 2013;31(22):2783-2790. 7. Prosigna [CE-IVD Package Insert] South San Francisco, CA: Veracyte, Inc; 2022-05 LB-0032-0 8. Parker JS, et al. J Clin Oncol. 2009;27(8):1160-1167. 9. Perou M, et al. Nature 2000; 406(6796):747–752 10. Cejalvo JM et al.Cancer Treat Rev. 2018 Jun;67:63-70. 11. Goldhirsch A, at al. Annals of Oncology 2013;24: 2206–2223.